Manual de mantenimiento de albercas
Una piscina que no se encuentre
químicamente equilibrada puede
producir irritaciones en la piel e
infecciones de oídos además de no
cumplir con la normativa vigente. La
legislación exige que las bacterias
nocivas y algas sean estrictamente
controladas mediante la utilización
de desinfectantes y ácidos.
PH
El pH es una medida de la acidez o alcalinidad del agua. Su expresión viene dada por el logaritmo negativo de la concentración del ion H+ expresada
en moles/ litro.
El agua pura neutra tiene una concentración de ion hidrógeno de 10
-7
moles por litro, luego el pH será de 7.
Una disolución ácida tiene mayor concentración de ion hidrógeno que el agua pura y por lo tanto su pH será menor que 7. Una disolución básica le
ocurre a la inversa y su pH será mayor de 7. Las medidas prácticas del pH se encuentran entre los valores 0 y 14.
En la medición del pH se pueden utilizar varios métodos, siendo el más exacto y versátil el sistema de electrodo de vidrio.
La medida de pH de una disolución se basa en la transformación de la señal eléctrica obtenida por un electrodo de vidrio y uno de referencia. Dicha
señal es proporcional a la actividad de los iones H
+
, de acuerdo con la ley de Nernst.
Valores indicativos
Los niveles aceptables de pH para el agua de la piscina están entre 7 y 7,8 nivel que asegura la eficacia de los productos químicos que se utilicen en
el tratamiento y que previene la corrosión de las partes metálicas del equipo de depuración. Un exceso o un defecto puede disminuir la eficacia de la
cloración e irritar las mucosas, además de contribuir al enturbiamiento del agua.
Corrección del pH
pH elevado (>7,8)
- Produce una disminución del poder desinfectante del cloro.
- Favorece el crecimiento de algas y bacterias.
- Produce irritación de mucosas.
- Precipitación de sales cálcicas.
pH bajo (<7,0)
- Produce irritación de mucosas.
- Aumenta el poder oxidante del cloro.
- Aumenta la turbidez del agua
Para aumentar el pH es necesario añadirle un producto alcalino:
• Carbonato de sodio
• Bicarbonato de sodio
Para disminuirlo, se debe añadir un producto ácido:
• Ácido clorídrico, salfumán
• Bisulfato sódico.
Puntos a tener en cuenta:
• No añadir nunca el agua encima del ácido. El ácido debe diluirse en un gran volumen de agua.
• Evitar, sobre todo, el contacto entre el ácido clorhídrico y el hipoclorito de sodio, ya que se desprende cloro gas.
• La adición de correctores se efectúa mediante bombas dosificadoras conectadas al circuito de recirculación después del filtro.
Para medir el PH necesitaremos un tester de ph

Qué es el Cloro?
Los productos clorados son las sustancias utilizadas con mayor frecuencia en el tratamiento químico del agua. Todos los productos clorados utilizados
en el tratamiento producen ácido hipocloroso(HClO) al reaccionar con el agua. La cantidad de ácido hipocloroso está muy condicionada por el valor
de pH.
En las aguas con un pH alto, la mayor parte de este ácido (cloro activo) se convierte en ión hipclorito (ClO-), una forma de cloro con muy bajo poder
desinfectante.
Estas dos formas de cloro se encuentran en el agua en equilibrio, aunque éste depende de los valores de pH.
Cloro libre: Esta forma de cloro posee el mayor poder desinfectante y oxidante, corresponde, fundamentalmente, a la presencia de ácido hipocloroso
y anión hipoclorito.
Cloro combinado: Tiene un poder desifectante muy bajo y su presencia causa irritaciones y malos olores. La combinación del cloro libre con el amoníaco
y la materia orgánica nitrogenada que contiene el agua, da lugar al cloro combinado (cloraminas).
Cloro total: La suma de cloro libre y el cloro combinado da como resultado el cloro total.
Por que medir el Cloro - Valores indicativos
La desinfección permanente del agua es necesaria y tiene dos finalidades:
Higiénica: Destruir los virus, bacterias, parásitos, etc. y eliminar los riesgos de contaminación.
De seguridad: Impedir el crecimiento de algas y mantener el agua limpia. El agua sin desinfectante, aunque no se utilice, se deteriora pronto por la
proliferación de algas y bacterias.
El cloro libre puede oscilar entre 0,5 mg/l y 2 mg/l. El cloro total no superará más de 0.6 mg/l el nivel medido de cloro libre.
Con un valor del pH de 4 (agua muy ácida), la cantidad de ácido hipocloroso presente es del 100%, lo cual es perfecto, si no fuera por el pH tan agresivo
que no permitiría el baño.
En el otro extremo, con un pH de 11 (agua muy alcalina), el 100% se corresponde a ión hipoclorito, lo cual es fatal a nivel de desinfección.
Los márgenes de pH aconsejados para la piscina por motivos de salud, de mantenimiento y de ahorro de cloro son entre 7.2 y 7.8:
- A un pH de valor 7.0 la concentración el ácido hipocloroso es del 75.2% del cloro libre.
- A un pH de 7.5 el ácido hipocloroso decrece hasta el 48.93%.
Acido isocianurico
El cloro libre se descompone rápidamente por la acción de los rayos ultravioletas del sol, perdiendo sus propiedades desinfectantes. Por otro lado, el ácido isocianúrico protege el cloro residual libre de las propiedades de descomposición de la luz solar. Este ácido no es un desinfectante, sino que
actúa como filtro de los rayos ultravioleta del sol, evitando la descomposición del ácido hipocloroso y, por tanto, el consumo inútil de cloro.
Este ácido isocianúrico es un producto estabilizante que actúa óptimamente en un intervalo de entre 25 y 50 gr/m3. El valor máximo es de 75 mg/l.
Por lo tanto, los productos clorados estabilizados son aquellos que contienen ácido isocianúrico, como el ácido tricloroisocianúrico y el dicloroisocianurato
de sodio.
Para medir el nivel de cloro necesitaremos un fotómetro de cloro

Qué es el Bromo / Ozono?
El bromo es un elemento químico que pertenece, al igual que el cloro, a la familia de los halógenos; tiene características y propiedades similares al
cloro. El bromo al mezclarse con el agua reacciona y se convierte en ácido hipobromoso. (HBrO) que es su forma activa de desinfección.
Las diferencias relevantes que resultan de la comparación con el cloro son:
- Tiene una mayor tolerancia a la variación de pH.
- No desprende olores desagradable.
- Mayor coste económico que el cloro.
- Menor eficacia que el cloro.
El ozono es el desinfectante más potente que se conoce, el único que responde realmente ante los casos difíciles (presencia de amebas, etc.). La
coloración del agua tratada con ozono produce un azul realmente bonito; no comunica ni sabor ni olor al agua; el ozono en ningún caso provoca
fermentación de productos que irritan las mucosas. Es conveniente mantener un pequeño residual de ozono en el agua, o en contrapartida añadir
un desinfectante como cloro o hipoclorito sódico en muy pequeñas cantidades que harán, por su mayor duración, un mantenimiento del agua más
prolongado.
La mayor desventaja del ozono es que requiere de una instalación costosa. Por el contrario, no requiere ningún gasto en reactivos.
Valores indicativos
La desinfección permanente del agua es necesaria y tiene dos finalidades:
Higiénica: Destruir los virus, bacterias, parásitos, etc. y eliminar los riesgos de contaminación.
De seguridad: Impedir el crecimiento de algas y mantenerla limpia. El agua sin desinfectante, aunque no se utilice, se deteriora pronto por la proliferación
de algas y bacterias.
Los valores indicativos o guía para el bromo libre activo oscilan entre 1.0 y 3.0 mg/l.
Para el ozono, se recomienda una concentración máxima antes de la desionización de 0.4 mg/l, y en el vaso de la piscina debe ser de 0.0 mg/l de ozono.
Otros métodos
Electrólisis de sal: Es equivalente al convencional de cloro, pero en la electrólisis se produce el cloro en la misma instalación, en función de las
necesidades. Tiene los mismos problemas que una instalación convencional de cloro. Su implantación es más económica que la de un sistema de
ozonización.
Lámparas UV: No se añade ningún componente al agua pero la depuración mediante UV no es tan exhaustiva como la realizada con ozono. Va a hacer
falta seguir dosificando una cierta cantidad de cloro. También resulta menos costosa su implantación que un sistema de ozonización.
Para medir el Bromo necesitaremos un Fotómetro de bromo

Para medir el ozono necesitaremos un Kit test de ozono
Qué es la Conductividad y TDS?
Se define la conductividad eléctrica como la capacidad de una sustancia de conducir la corriente eléctrica. Es indicativa de la materia ionizable y
de la cantidad de sales disueltas presentes.
La conductividad es directamente proporcional a la concentración de sal en el agua. Cuando el nivel de sal disminuye, la conductividad también
disminuye. La unidad de medida más utilizada es el microsiemens.
Utilizando medidores de conductividad se puede calcular la dureza del agua con mediana precisión. La causa principal de la dureza del agua es la
presencia de iones de calcio o magnesio disueltos.
La unidad de medición de dureza más común es el º Francés (ºf), definido como:
1ºf = 10 mg/l de CaCO3
Otra relación experimentada es:
1mg/l de CaCO3 equivale aproximadamente a 2 uS/cm = 1ºfrancés equivale a 20 uS/cm
El TDS indica la totalidad de materia que está disuelta en el agua que corresponde a la materia que quedaría si toda el agua se evaporase.
Los sólidos disueltos totales lo componen substancias disueltas como son las sales minerales, los productos químicos añadidos, polvo, tierra y
substancias introducidas por los bañistas (orina, sudor, cremas, etc...)
Valores indicativos
El valor límite de la conductividad es de 1.200 – 1.700 uS/cm.
La conductividad y los TDS reflejan con buena precisión el momento de cambiar una parte del agua de la piscina por un agua “nueva”. Para una
conductividad superior a 1.200 uS/cm sería interesante reemplazar parte del agua del vaso de la piscina.
Un agua potable puede tener aproximadamente entre 200 y 400 gramos de sólidos disueltos por cada m3, el agua salobre contiene entre 3.000 y
5.000 mg/l y el agua de mar 35.000 mg/l por la gran cantidad de sales que tiene disueltas, principalmente, cloruro de sodio (NaCl). Las piscinas de
agua dulce no deben sobrepasar un TDS de 1.000 mg/l, aunque es recomendable no superar los 500 mg/l.
Cuando un agua tiene un nivel excesivo de TDS se le denomina “agua cansada” y puede provocar problemas como la reducción de la efectividad
del desinfectante, el aumento de la turbidez, las incrustaciones y la corrosión de las partes metálicas.
La disminución de la conductividad y de los sólidos disueltos totales (TDS) se debe efectuar reemplazando una parte del agua de la piscina con agua
nueva que tendrá poca cantidad de sólidos disueltos.
Medidor de conductividad

Qué es el Potencial Redox?
El Redox se refiere a un tipo de reacciones en las que las sustancias participantes se intercambian electrones. En ellas, coexisten dos procesos:
- Oxidación: Pérdida de electrones.
- Reducción: Ganancia de electrones.
Cuando una sustancia pierde electrones, otra los tendrá que ganar y al revés. Los procesos de oxidación y de reducción tienen que ir necesariamente
ligados. Por eso se habla de reacciones de reducción-oxidación o REDOX.
Se denomina oxidante la sustancia que produce la oxidación de otra sustrayéndole electrones. La ganancia de estos electrones produce la reducción
del oxidante.
Se denomina reductor la sustancia que produce la reducción de otra cediéndole electrones. La cesión de estos electrones produce la oxidación del
reductor.
Los oxidantes son normalmente cáusticos y los agentes reductores son normalmente ácidos. La medida del potencial redox depende del pH.
Valores indicativos
El Redox es una medida rápida y económica del poder de desinfección de los biocidas oxidante.
Los instrumentos que miden Redox son válidos para el cloro, bromo y ozono.
El potencial Redox nos da información sobre el grado de desinfección del agua de la piscina. La Organización Mundial de la Salud dice que a un valor
de ORP superior a 650 mV, el agua se encuentra perfectamente desinfectada y es inactivada.
Que es la Temperatura
La temperatura del agua de piscina puede variar entre 20ºC y 30ºC según los Reglamentos Autonómicos. Desde el punto de vista de HANNA Instruments,
la temperatura recomendada oscilara entre 24ºC y 28ºC y de 27ºC a 30ºC para la temperatura del ambiente.
Por debajo de los 18ºC se considera agua fría y sin problemas; sobre los 24ºC puede presentar precipitaciones de sales cácicas y enturbiamiento.
Cuanto más alta sea la temperatura más se desarrollan las bacterias, algas y otros microorganismos.
Los recintos interiores dispondrán de instalaciones que garanticen la renovación del aire del recinto manteniendo un volumen de 8m3 de aire por m2
de superficie de lámina del agua.
Medidor de ORP y Temperatura
La oxidación es un proceso en el que una molécula o ion pierde electrones. Esto sucede muy fácilmente en los
tratamientos de agua así como en el mantenimiento de piscinas y balnearios donde se añade un oxidante como
el cloro al agua para destruir contaminantes. Cuanto más positivo sea el valor ORP, tanto mayor será el poder
de esterilización del agua. El tester de ORP puede facilitar una valiosa información sobre la calidad de las aguas.


Qué es la Dureza y la Alcalinidad?
La dureza indica la cantidad de sales de calcio y de magnesio disueltas en el agua. Se expresa en gramos de carbonato de calcio por cada metro
cúbico de agua. También se expresa en grados hidrotrimétricos franceses.
La alcalinidad indica la cantidad de substancias alcalinas (carbonatos, bicarbonatos y hidróxidos) que contiene el agua.
Los componentes alcalinos que contiene el agua actúan como reguladores del pH del agua. Esto significa que una alcalinidad adecuada garantiza
que el pH se pueda mantener prácticamente constante cuando se añaden pequeñas cantidades de ácido o de base.
La alcalinidad se expresa en gramos de carbonato de calcio por cada m3 de agua. También se expresa en grados hidrotrimétricos franceses.
1ºFrancés equivale a 10 mg/l de carbonato cálcico (grCaCo3/m3).
Valores indicativos
Una dureza muy baja puede producir daños en el vaso de la piscina y corrosión en las partes metálicas en contacto con el agua (escaleras, focos,
etc). Por el contrario, una dureza excesiva puede producir turbiedad en el agua, incrustaciones, obturación de los filtros y las tuberías, rugosidades
y manchas en la superficie de la piscina.
Si la alcalinidad es muy baja resulta muy difícil la regulación del pH, ya que el agua es muy sensible a ligeras variaciones. Además puede favorecer
la corrosión y la aparición de manchas en las partes metálicas. Una alcalinidad excesivamente alta produce incrustaciones, agua turbia, pH elevado
e irritaciones de las mucosas de los bañistas.
Los valores indicativos son:
La dureza ideal oscila entre 150 y 250 mg/l.
La alcalinidad aconsejada oscilará entre los 125 y 150 mg/l
La dureza puede aumentarse añadiendo cloruro cálcico. En el caso de que sea necesario disminuir la dureza, puede conseguirse sustituyendo una
parte del agua de la piscina por otra agua de menor dureza. Asimismo, este objetivo puede alcanzarse incorporando al agua un agente quelante o
secuestrante que ayude a mantener disueltas las sales de calcio.
La alcalinidad se puede aumentar añadiendo al agua carbonato o bicarbonato sódico (sustancias alcalinas) y disminuir diluyendo bisulfato sódico
o ácido clorhídrico (sustancias ácidas).
Tanto la dureza como la alcalinidad se deben controlar en la propia piscina. En caso de dificultad se pueden realizar los análisis en un laboratorio.
Los dos parámetros son necesarios para conocer y calcular el equilibrio del agua por medio del Indice de Langelier.
Test Kit Alcalinidad

Qué es el Indice de Langelier? Equilibrio del Agua.
El índice de saturación desarrollado por el Dr. Wilfred Langelier se usa ampliamente para predecir el equilibrio de las aguas de las piscinas. Es un cálculo
estimativo de la capacidad de las soluciones para disolver o precipitar los depósitos de carbonato de calcio. Un cierto nivel de esta precipitación (película)
es conveniente para aislar las tuberías y calderas del contacto con el agua. Cuando no se forma esta película protectora, se considera que el agua es
corrosiva. Por otro lado, las incrustaciones causan fallos en el sistema.
Por tanto, el Indice de Langelier es una potente herramienta para calcular el equilibrio del agua y para predecir los problemas de corrosión e incrustaciónes.
Para el cálculo de este índice, se requiere conocer los valores de pH, temperatura, alcalinidad y dureza aplicándose la siguiente fórmula:
IL=pH + TF + HF + AF – 12,5
Donde, IL=Indice de Langelier / pH = pH del agua / TF = factor de temperatura / HF= factor de dureza / AF= factor de alcalinidad.
Estos factores se pueden obtener en la siguiente tabla:
TEMPERATURA |
DUREZA |
ALCALINIDAD |
ºC |
TF |
ppm |
HF |
ppm |
AF |
0 |
0,0 |
5 |
0,7 |
5 |
0,7 |
4 |
0,1 |
25 |
1,4 |
25 |
1,4 |
8 |
0,2 |
50 |
1,7 |
50 |
1,7 |
12 |
0,3 |
75 |
1,9 |
75 |
1,9 |
16 |
0,4 |
100 |
2,0 |
100 |
2,0 |
20 |
0,5 |
150 |
2,2 |
150 |
2,2 |
24 |
0,6 |
200 |
2,3 |
200 |
2,3 |
28 |
0,7 |
250 |
2,4 |
250 |
2,4 |
32 |
0,7 |
300 |
2,5 |
300 |
2,5 |
36 |
0,8 |
400 |
2,6 |
400 |
2,6 |
40 |
0,9 |
500 |
2,7 |
500 |
2,7 |
50 |
1,0 |
1000 |
3,0 |
1000 |
3,0 |
Ejemplo de cálculo

La interpretación del resultado obtenido al aplicar la fórmula de cálculo del IL es la siguiente:
- Si el índice es cero, indica que el agua está perfectamente equilibrada.
- Si el índice es negativo, indica que el agua tiene tendencias corrosivas.
- Si el índice es positivo, significa que el agua tiene tendencias incrustante.
Los valores del IL se consideran absolutamente óptimos en el intervalo ( - 0.3, + 0.3) y aceptables entre ( - 0.5 y + 0.5)
Medidor del Indice de Langelier
Este instrumento utiliza un sistema de cierre exclusivo para garantizar que la
cubeta está en la misma posición cada vez que se sitúa en la célula de medida.
Los reactivos, en forma líquida o en polvo, se suministran en botellas o en
sobres. La cantidad de reactivo está dosificada con precisión para garantizar
la máxima repetibilidad.
Los códigos de pantalla ayudan al usuario en las operaciones rutinarias.
Dispone de una función de auto-apagado, que desconecta la unidad tras 10
minutos de inactividad.
Qué es la Turbidez?
La turbidez es una medida del total de luz absorbida por el agua, a causa de la materia suspendida en la misma. Es una expresión de la propiedad óptica
que origina que la luz se disperse y absorba en vez de transmitirse en línea recta de la muestra.
Es un claro indicador del buen funcionamiento del sistema de tratamiento del agua de la piscina y en general de la eficacia de la depuración.
Los resultados se expresan en NTU (Unidades Nefelométricas de turbidez)
El hierro se encuentra en las aguas naturales bajo dos formas:
- En estado mineral ( sales Ferrosas = Fe 2+ y sales férricas = FeCl3 ó hidróxido = Fe (OH3).
- En estado orgánico (coloides).
El agua turbia produce una turbidez alta y suele ser consecuencia de un pH alto y/o una alcalinidad alta, una filtración pobre, unas contracorrientes
ineficaces y formación de algas. La turbidez alta da irritación en los ojos, reduce el efecto biocida del cloro o el desinfectante utilizado y aumentan la
incrustación.
Qué es el Hierro?
El hierro es un indicador de la corrosión del agua en el circuito de la piscina. La estabilidad de las distintas formas químicas depende del pH y de las
condiciones oxidantes o reductoras del medio.
La presencia del hierro en el agua provoca precipitación y coloración no deseada. Las sales de hierro y
manganeso producen un color marrón. Las sales de cobre producen una coloración azul/verde.
El valor indicativo de la turbidez será igual o inferior a 2 NTU.
Los metales disueltos en el agua, entre otros, son responsables de dar una coloración a las aguas.
Una baja alcalinidad también produce un color verde en el agua.
El tratamiento que ha de llevarse a término será:
- Ajustar el pH entre 9 y 10. Los compuestos metálicos precipitan.
- Efectuar una cloración de choque.
- Flocular
- Enviar la basura al desague con el limpiafondos al cabo de unas horas.
- Filtrar
- Ajustar el pH entre 7,2 y 7,6 cuando el agua se haya recuperado

Dosificación, medición y regulación automática
La dosificación de reactivos será siempre automática para todos los vasos de las piscinas.
La dosificación del desinfectante y el corrector de pH se realizará después del filtro y a una distancia suficiente del vaso, con objeto de que se mezcle en condiciones y no produzca molestias a los bañistas. El floculante se adicionará previo a la filtración.
Se aconseja colocar los electrodos para la toma de medidas a la salida del depósito de compensación, con objeto de tener una
lectura lo más aproximada al valor real del agua en el vaso de la piscina.
La medida directa de cloro libre se realiza mediante analizadores colorimétricos por DPD o por sondas galvánicas autolimpiantes.
En el método colorimétrico DPD, el indicador N, N-Dietil-p-fenilendiamina y la solución se mezclan con la muestra; el Cloro Libre disponible se oxida con el reactivo indicador DPD a un pH entre 5.5 y 6.0 para formar un compuesto color magenta. La intensidad del color resultante es proporcional a
la concentración de la muestra. El propósito del reactivo tampón es el de mantener el pH adecuado.
La medida con la sonda galvánica autolimpiante utiliza la capacidad de oxidación que posee el cloro u otros biocidas oxidantes.
La medición de pH se origina en el sistema del electrodo. Este sistema consiste en un sensor de pH, cuyo voltaje varía proporcionalmente a la actividad de iones de hidrógeno de la solución, y un electrodo de referencia, que proporciona un voltaje de referencia constante y estable.
La dosificación del ácido y del cloro líquido se realiza por medio de dos bombas dosificadoras que incorporan los productos procedentes de los filtros.
Medidores, reguladores en continuo


Valores indicativos de la Calidad del Agua en piscinas
Cada Comunidad Autónoma ha elaborado un Decreto donde se establecen las condiciones higiénico sanitarias aplicables a piscinas de uso colectivo
donde se exponen los valores de los parámetros fisico-químicos del agua de la piscina.
Por parte del Ministerio de Sanidad se publicó el R. Decreto 865/2.003 del 4 de julio, por el que se establecen los criterios higiénicos sanitarios para
la prevención y control de la legionelosis. En el se clasifica las bañeras de hidromasaje y piscinas como instalaciones de mayor probabilidad de
proliferación y dispersión de legionella. Indicando como debe ser el diseño, revisión, limpieza y desinfección de estas.
En la siguiente tabla se presentan los valores indicativos de los parámetros físico-químicos más importantes en la piscina.
Valores Recomendados:
| |
Valor mínimo |
Valor máximo |
| pH |
7,0 |
7,8 |
| Cloro Libre (mg/l) |
0,5 |
2,0 |
| Cloro combinado (mg/l) |
-- |
0,6 |
| Bromo total (mg/l) |
3,0 |
6,0 |
| Biguanida (mg/l) |
25 |
50 |
| Acido isocianúrico (mg/l) |
-- |
< 75 |
| Ozono (vaso ) (mg/l) |
-- |
0 |
| Ozono (antes de ) |
0,4 |
-- |
| Temperatura del agua ºC |
24 |
30 |
| Turbidez (NTU) |
-- |
< 1 |
| Oxidabilidad (mg/l) |
-- |
< 3 |
| Nitratos (mg/l) |
-- |
< 20 |
| Amoniaco (mg/l) |
-- |
< 0,3 |
| Hierro (mg/l) |
-- |
< 0,3 |
| Cobre (mg/l) |
-- |
< 1,5 |
| Alcalinidad (mgCaCO3/l) |
100 |
160 |
| Conductividad (uS/cm) |
-- |
<1700 |
| TDS (mg/l) |
-- |
< 1000 |
| Dureza (mg/l) |
150 |
250 |
Diferentes formas de Cloro en el agua
El ácido hipocloroso es la forma activa del cloro, el cual le da el poder desinfectante. Para poder tener una concentración adecuada
es importante que el pH se encuentre dentro de unos márgenes. Se recomienda que el pH se mantenga entre 7,0 y 7,8.
El cloro necesario para mantener un óptimo poder desinfectante está en función del pH, como muestra la tabla siguiente:
| pH |
7,0 |
7,4 |
7,7 |
7,9 |
| Cloro residual libre |
|
| necesario (mg/l) |
|
|
|
|
El cloro residual libre puede oscilar entre el 0,5 y 2 mg/l. El cloro total no debe sobrepasar más del 0,6 mg/l del nivel de cloro residual
libre.
Cloro residual:
Fracción de cloro añadido que conserva las propiedades desinfectantes.
Cloro residual libre:
Cantidad de cloro presente en el agua en forma de ácido hipocloroso o hipoclorito.
Cloro residual combinado:
Cantidad de cloro presente en el agua en forma de cloraminas o de otros compuestos orgánicos del cloro.
Cloro residual total:
Suma del cloro residual libre y del cloro residual combiando.
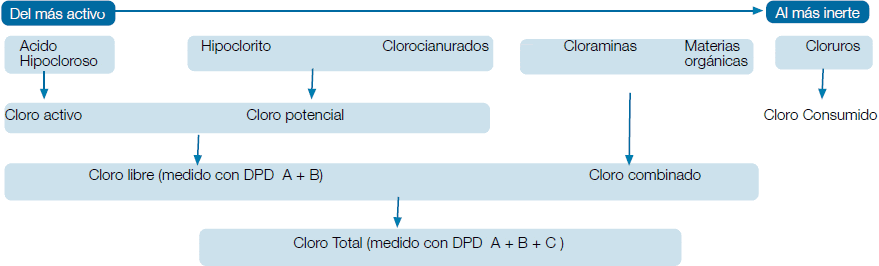
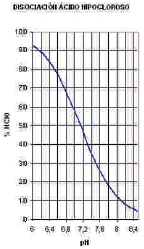
Gráfica del % de Cloro activo en función del pH
La cantidad de ácido hipocloroso presente en el agua está muy condicionada por el valor del pH. En las aguas con un pH alto, la mayor
parte del cloro activo se convierte en ion hipoclorito, (ClO), una forma de cloro con muy bajo poder desinfectante. El ácido hipocloroso
tiene mayor poder oxidante y bactericida que el ion hipoclorito, por lo que, es importante mantener un valor de pH adecuado para
obtener una desinfección eficiente. En las aguas con un pH básico, disminuye el porcentaje de ácido hipocloroso, y aumenta el del
ion hipocloríto con un poder oxidante inferior, de manera que disminuye el poder desinfectante del agua. El valor de pH idóneo para
obtener una mayor desinfección es entre 7.0 y 7.2.
| pH |
% cloro activo |
% cloro inactivo |
| 6,0 |
95 |
5 |
| 6,5 |
90 |
10 |
| 7,0 |
75 |
25 |
| 7,2 |
66 |
34 |
| 7,5 |
47 |
53 |
| 8,0 |
22 |
78 |
| 8,5 |
8 |
92 |
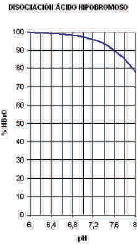
A diferencia de lo que sucede con el ácido hipocloroso, la cantidad de ácido hipobromoso presente en el agua varia muy poco con
los cambios del pH.
Tal y como se observa en la siguiente gráfica:
| pH |
% bromo activo |
%bromo inactivo |
| 6,0 |
100 |
0 |
| 7,0 |
98 |
2 |
| 7,2 |
96 |
4 |
| 7,8 |
87 |
13 |
| 8,0 |
83 |
17 |
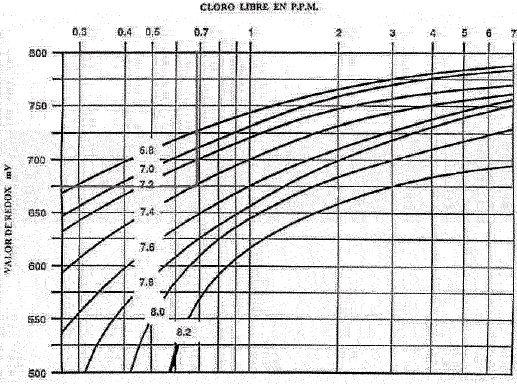
Relación Redox - pH - Cloro
La tecnología de la lectura de ORP para controlar un desinfectante ha sido reconocida e incorporada en Europa y en el mundo del agua desde hace
años. En 1972, la Organización Mundial de la Salud reconoció en sus "Standards for Drinking Water (WHO1972) que un nivel de ORP de 650 mV en el
agua desinfecta e inactiva viralmente de forma casi instantánea.
Alemania, que tiene algunos de los estándares más restrictivos de la calida del agua en el mundo, ha fijado su estándar en 750 mV para las piscinas y
los balnearios. En 1988, el Instituto Nacional del Balneario y de la Piscina (NSPI) indicó que el ORP se podría utilizar como medida suplemental de la
actividad apropiada de la esterilización cuando el cloro y el bromo se utilizan como el desinfectante primario. El NSPI también indicó que el uso de la
medida de ORP no reemplaza ni elimina la prueba de los niveles con los kits estándares.
Diferentes estudios han demostrado que un valor de ORP de 650 a 700 mV medidos entre 6,5 y 8,5 provocan la eliminación de microorganismos
patógenos. En estudios realizados hasta la fecha apuntan fuertemente el uso de 650 mV como valor umbral mínimo para una actividad antibacteriana
típtica. Este valor de 650 mV es consistente con las normas que fueron desarrolladas y han sido utilizadas en Europa desde mediados de 1980 para la
calidad del agua potable municipal.
Se debe tener en consideración que las medidas de ORP dependen del valor de pH. Por ejemplo, la cantidad de ácido hipocloroso existente en el agua
varía en función del pH, ya que se forma el ión hipoclorito. Un aumento del pH provoca una disminución del ORP. Este problema no se tiene en las
piscinas ya que el pH el agua está controlado y es poco variable.
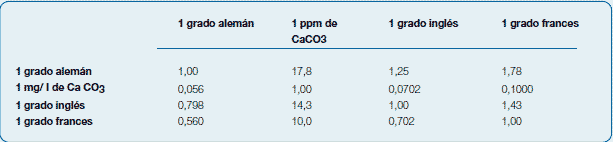
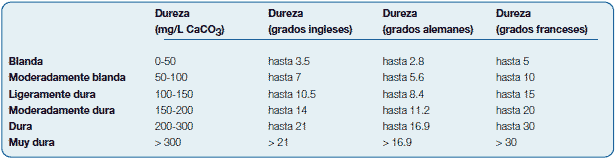
Tablas de conversión de Dureza
El contenido total de sales incrustantes existentes en el agua se mide por el grado hidrotimétrico de dureza. En Europa, dependiendo del país, existen
grados Franceses (ºf), grados Alemanes ( ºD) y grados ingleses. (ºE). En España se emplea el grado Francés.
A continuación indicamos una tabla de conversión de las diferentes unidades de expresión de la dureza:
Clasificación del agua en función de la dureza
El inconveniente más grave que presentan las aguas duras es la precipitación de las sales cálcicas y magnésicas formando incrustaciones. Las tuberias
por las que circula el agua dura ya sea fría o caliente, se van obstruyendo con la consecuente disminución de su sección útil. En las instalaciones de
bombeo se requieren mayores potencias para obtener las mismas condiciones de caudal y presión.
Preguntas y respuestas más frecuentes
¿A qué es debido el aspecto verdoso o parduzco del agua? ¿Cómo se puede solucionar?
A la excesiva presencia de iones metálicos, los cuales se colorean al añadir el desinfectante. Se debe controlar el pH, ajustándolo
entre 7,2 y 7,8. Realizar una supercloración y cepillar paredes y fondo de la piscina.
¿A qué es debido el fuerte olor de cloro y picazón de ojos? ¿Cómo se puede solucionar?
A la excesiva presencia de cloro combinado es decir cloraminas y a la materia orgánica. Se debe ajustar el pH entre 7,2 y 7,8,
medir el cloro libre (método DPD) y realizar una cloración de choque.
Una piscina desinfectada, ¿puede perder el cloro después de filtrarse el agua?
No, no se pierde el cloro. Si el filtro está sucio, es decir tiene un alto contenido de materia orgánico disminuirá la cantidad de
cloro al pasar por el filtro ya que el cloro reacciona con la materia orgánica presente en el filtro.
¿Cada cuánto tiempo se debe clorar el agua de una piscina si no se utiliza a menudo?
Se debe controlar el cloro libre (método DPD) y el pH para observar si los valores son los establecidos en la legislación. Se
deben corregir si son diferentes a los establecidos.
¿A qué es debido la aparición de cal? ¿Cómo se puede solucionar?
A un agua dura y a un pH alto, con el cual la cal se hace visible y precipita. Se debe realizar una floculación. Se para el filtro
y se deja que sedimente los sólidos de la piscina. Después de 24 horas se pasa el limpiafondos. Se deberá ajustar el pH entre
7,2 y 7,8 y seguir con el tratamiento habitual.
¿A qué es debido la aparición de algas en el agua? ¿Cómo se puede solucionar?
La cantidad de algicida es insuficiente, y/o puede ser excesiva la cantidad de nutrientes (fosfatos) que facilitan el crecimiento
de algas. Se debe limpiar a contracorriente el filtro y eliminar las algas con un cepillado, seguidamente se debe ajustar el valor
de pH y realizar un tratamiento de choque. Se debe adicionar floculante y se filtrará durante dos días. A continuación se
adicionará una cantidad doble de algicida.
¿Cómo afecta a la piscina una alcalinidad alta?
Una alcalinidad superior a 225 mg/l dificultará la estabilidad del pH y producirá corrosión en las instalaciones. El agua tomará
un tono verde que le causará irritaciones en los ojos. Para solucionar deberá añadir ácido clorhídrico o bisulfito sódico.
¿Cómo afecta a la piscina una alcalinidad baja?
Una alcalinidad inferior a 75 mg/l dificulta la estabilidad del pH. Se produce por las características del agua de aporte o llenado
y por las adiciones de producto químico. Para resolver el problema se añadirá al agua de la piscina bicarbonato sódico o
carbonato sódico.
Mantener
básico de
la piscina
Herramientas de limpieza
Desinfectante

Reguladores de PH
Productos complementarios
Al empezar la temporada
SI PREPARASTE LA PISCINA PARA EL INVIERNO PASADO
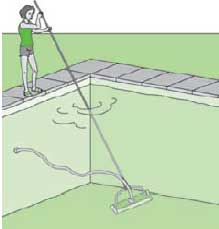
1.- Limpiar las paredes y el fondo del vaso
2.-Si es necesario, éste es el mejor momento
para reponer alguna pieza de gresite que
se haya desprendido o reparar posibles
fisuras en el material del vaso. |
 |
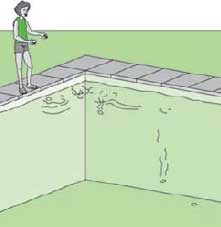
3.- Comprobar los niveles de desinfectante y
pH y utilizar un tratamiento de choque
para corregirlos.
|
 |
4.- Completar la limpieza, aplicando algicida
y floculante disueltos en agua alrededor
del perímetro de la piscina .
|
 |
SI NO REALIZASTE UN INVERNAJE ADECUADO
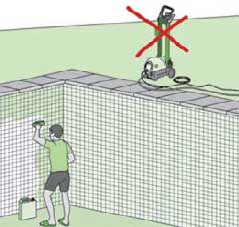
1.- Vaciar la piscina y limpiar las paredes y el
fondo con un producto desincrustante.
Si la piscina es de gresite, procura no
utilizar una limpiadora a presión. |
 |
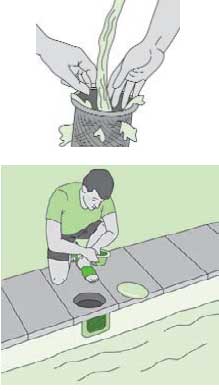
2.- Limpiar los skimmers, los filtros, las boquillas de
impulsión, etc.
|
 |
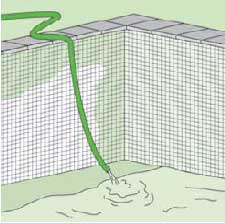
3.- Colocar la manguera en el fondo para
que se vaya llenando. Iniciar así el
llenado de la piscina evita que se dañe el
revestimiento del fondo del vaso.
|
 |
4.- Seguir los pasos 3 y 4 del apartado anterior
|
|
Durante la temporada
CLAVES PARA EL MANTENIMIENTO
Mantener a punto el agua de la piscina, es decir, transparente y limpia,
te exige realizar de forma periódica una serie de tratamientos físicos
(limpieza y filtrado) y químicos (desinfección).
1. Para la filtración, son necesarios:
a) Recogehojas y limpiafondos.
b) Sistema de recirculación y filtrado (mediante “la depuradora”).
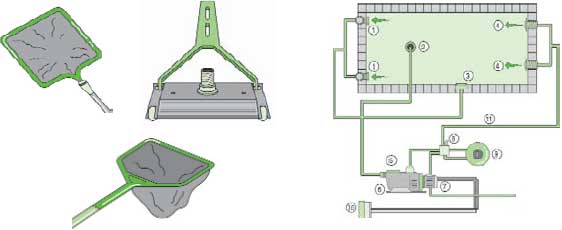
2. Para la desinfección, se emplean distintos productos químicos:
a) Desinfectantes:
Cloro, bromo u oxígeno activo.
b) Reguladores del pH:
- Reductores del pH.
- Elevadores del pH.
c) Productos complementarios:
- Algicida y anticalcáreo.
- Floculante.
- Desincrustantes-limpiadores.

A. ELEMENTOS DE LA DEPURADORA Y SU MANTENIMIENTO
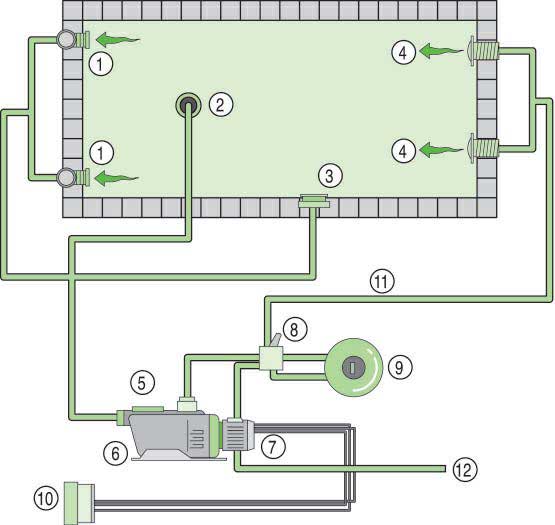
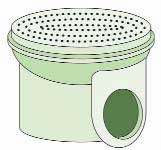
Skimmer
Recoge el agua para su filtrado en la superficie de la
piscina.
Limpiar el cesto semanalmente.
El rebosadero es un sistema
alternativo al skimmer que
recoge el agua a lo largo de
todo el perímetro de la piscina. La conducción se limpia una vez
a la semana.
Sumidero
Recoge el agua para su filtrado en el fondo del
vaso y permite, además, el vaciado de la piscina (a
través del circuito o directamente al desagüe).
Boquilla de aspiración
Conecta la toma del limpiafondos al circuito de
filtrado.
Boquilla de impulsión
Permite la salida del agua de la depuradora a la
piscina.
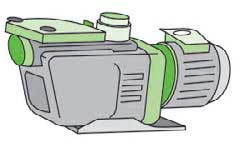
Prefiltro + Bomba + Motor
Posibilita el transporte del agua en el
circuito.
Limpiar el prefiltro semanalmente y seguir el
mantenimiento indicado por el fabricante.
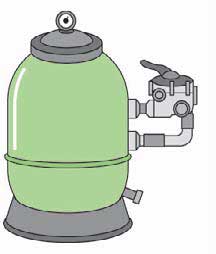
Válvula de 6 vías + Filtro
El filtro permite la eliminación de elementos
sólidos y de algunos de los elementos en
suspensión de la piscina.
La válvula controla las diferentes funciones del
circuito (descritas en el apartado siguiente de esta
misma ficha).
Lavar y enjuagar el filtro una vez a la semana.
Verificar las válvulas mensualmente.
Una vez al año, verificar el nivel del lecho de
filtrado y desincrustar con un ácido débil.
Cambiar el lecho de filtrado cada 4-6 años.
Armario eléctrico
Posibilita la automatización del funcionamiento
del sistema de filtrado del agua.
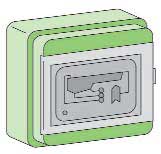
Tubería flexible de PVC
Conecta todos los elementos del circuito y
permite también realizar el desagüe de la
piscina.
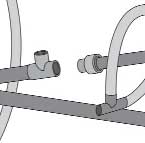
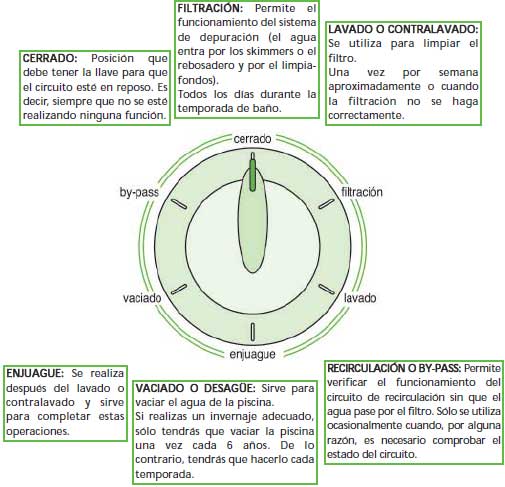
B. OPERACIONES DE RECIRCULACIÓN Y FILTRADO DE AGUA
A través de la llave de 6 vías puedes seleccionar las distintas operaciones
de mantenimiento.
A continuación aparecen las funciones y la periodicidad con la que debes
realizarlas:
Consejo
Las labores de limpieza de elementos sólidos comienzan por
el uso diario de los recogehojas. Por eso resulta muy cómodo
disponer de uno plano (para los elementos más superficiales)
y otro con bolsa para recogidas de mayor volumen.
C. DESINFECCIÓN DEL AGUA
Antes de proceder al mantenimiento químico de tu piscina, es
importante que calcules el volumen de agua que contiene. Sólo así
podrás estimar la dosis más apropiada de cada producto.
¿Cómo calcular el volumen de la piscina?
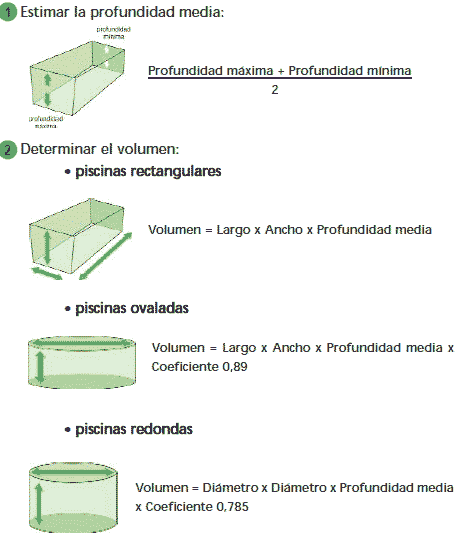
Los desinfectantes se presentan en diferentes concentraciones, formas
de aplicación (granulado, pastillas o líquido) y, en ocasiones,
acompañados de tratamientos complementarios (productos multifunción
y productos de invernaje).
Esta variedad de formulaciones te permite ajustar la rutina de limpieza
a las necesidades precisas de desinfección de tu piscina y, lo que también
es importante, a la cantidad de tiempo que tengas disponible. Así, si
utilizas productos más concentrados, tendrás que hacer menos
aplicaciones mensuales.
Atención: Los tratamientos químicos deben realizarse al atardecer o
por la noche y siguiendo siempre las instrucciones de
dosificación, forma de aplicación y recomendaciones de
protección (guantes, etc.) que se aconsejan para cada
producto.
En el siguiente cuadro aparecen las operaciones de mantenimiento
químico que exige el agua y la periodicidad con que conviene realizarlas.
| |
Desinfección
(Elige sólo uno de
ellos para tu piscina) |
Control pH |
Tratamientos
complementarios |
| |
Cloro |
Bromo |
Oxígeno |
Elevador del pH
Reductor del pH |
Algicidas, floculantes y
desincrustantes |
| A diario |
Comprobar el nivel de
desinfectante con los
equipos analizadores y
corregirlo aplicando la
dosis oportuna de
producto de acción
inmediata.
|
Comprobar el nivel
de pH y corregirlo
con la dosis de
regulador necesaria
en cada caso. Se
r e c o m i e n d a
mantener el pH entre
7 y 7,4.
|
|
Una vez a la
semana |
Reponer la dosis de
desinfectante necesaria
(en el caso de que se
estén utilizando productos
para mantenimiento
semanal, de
acción más lenta). |
|
Tras la primera
aplicación de algicida
de la temporada, se
repite el tratamiento
a la semana y después
cada 15 días. |
| Eventualmente |
En ocasiones, se puede producir un aumento de la turbiedad del
agua; así como un descenso en los niveles de cloro y una alteración
del nivel del pH. Las causas más habituales son: las tormentas, el uso
intensivo de la piscina, el aumento repentino de las temperaturas,
etc.
Para recuperar los niveles correctos, es necesario realizar una
aplicación de choque de cloro de acción rápida, corregir el valor del
pH y añadir líquido floculante (que elimina la turbiedad del agua). |
Solución a los problemas más habituales
| SÍNTOMAS |
CAUSA |
TRATAMIENTO |
| Agua verde |
Presencia de
algas o niveles
altos de cobre. |
-Ajustar el pH.
-Efectuar un tratamiento de
choque de desinfectante (cloro). |
| Agua blanquecina |
Desajustes del pH,
presencia de
contaminantes en
el agua y/o
suciedad del filtro. |
-Ajustar el pH.
-Aplicar un tratamiento de choque
y, si no hay mejora, verificar el
estado de las arenas del filtro. |
Paredes viscosas y
suelo resbaladizo |
Niveles bajos de
cloro y presencia
de algas. |
-Efectuar un tratamiento de
choque (los niveles de cloro deben
estar entre 0,8 y 1,4 ppm).
-Aplicar un tratamiento antialgas. |
Olor fuerte que
provoca irritación
de los ojos y
mucosidad |
Desajustes del
pH. |
-Medir y corregir el pH.
|
| Turbiedad del agua |
Presencia de
elementos en
suspensión. |
-Ajustar el pH.
-Aportar floculante y, si no mejora,
revisar el filtro. |
Al final de la temporada
Éstas son las operaciones que debes realizar nada más terminar la
temporada de baño para preparar el invernaje de tu piscina:
1.- Dejar el agua en buen estado con un contenido bajo de cloro libre.
2.- Con el circuito de filtrado en marcha,
añadir producto de invernaje.
3.- Parar el circuito al día siguiente, echar en
el agua un trozo de madera (o cualquier
otro elemento que flote) y cubrir la
piscina con una lona de invernaje.
Glosario de Términos
Acidez:capacidad cuantitativa de una solución acuosa para reaccionar con iones hidroxilos. Se mide por titulación con una solución estándar de una
base hasta el punto final especificado. Generalmente se expresa en miligramos de carbonato cálcico por litro.
Ácido: sustancia que tiene tendencia a perder un protón (H+).
Álcali: cualquier sustancia que posee propiedades marcadamente básicas. El término se suele aplicar a sales solubles de sodio, potasio, calcio y
magnesio.
Alcalinidad: capacidad del agua para neutralizar ácidos.
Anión: ión con carga negativa.
Bromo: compuesto halógeno que en contacto con el agua forma ácido hipobromoso con alto poder desinfectante, también forma bromaninas que al
contrario de las cloraminas desinfectan. El bromo activo, como desinfectante, es muy estable a las variaciones de pH.
Buffer: sustancia que estabiliza el pH de las soluciones.
Calibración: determinación, comprobación o rectificación de la graduación de cualquier elemento que se utilice para mediciones cuantitativas.
Cloración: aplicación de cloro o compuestos de cloro al agua generalmente con fines de desinfección, pero también para oxidación orgánica o control
de olores.
Cloramina (Cloro combinado): sustancia que se forma cuando se combina el ácido hipocloroso con compuestos nitrogenados.
Cloro libre: corresponde al cloro activo disponible después de haberse completado totalmente la desinfección. Esta forma de cloro, que posee el mayor
poder desinfectante y oxidante, corresponde fundamentalmente a la presencia de ácido hipocloroso y al anión hipoclorito.
Cloro total: suma de cloro libre y cloro combinado.
Colorímetro: instrumento que mide la cantidad de luz de una determinada longitud de onda que es absorbida por una solución.
Conductividad: capacidad de una sustancia de conducir la corriente eléctrica y es inversa de la resistencia eléctrica.
Conductivímetro: es el instrumento válido para medir la conductividad eléctrica. La lectura puede ser amperométrica o potenciométrica.
Desinfección: destrucción por medio de un agente desinfectante, como puede ser el cloro, de las bacterias patógenas y fecales y de virus transmitidos
por el agua que se encuentra en los suministros de agua potable y efluente de una estación depuradora de aguas residuales
Desinfectante: agente químico que destruye microorganismos, no así esporas bacterianas.
Dureza: característica del agua impartida principalmente por sales de calcio y magnesio, tal como bicarbonatos, carbonatos, sulfatos, cloruros y nitratos.
Se expresa en mg/L o en grados franceses, alemanes.
Indice de Langelier: medida del grado de saturación del carbonato de calcio en el agua, el cual se basa en el pH, alcalinidad y dureza. Si el índice es
positivo es un agua incrustante, si es negativo un agua corrosiva.
Indice de Ryznar: Similar al de Langelier y basado en los mismos parámetros. Si el índice de Ryznar tiene un valor de 6.0 o menor, el agua tiene tendencia
incrustante, con un índice de 7.0 la incrustación no ocurre. Cuando el valor aumenta a valores superiores de 7.5 a 8.5 se incrementa el problema de la
corrosión.
Intercambio iónico: proceso químico en el cual se intercambian iones de dos moléculas diferentes.
Ion: átomo o molécula que ha perdido o ganado uno o más electrones, la partícula se carga electricamente.
Método DPD: método analítico para determinar el cloro libre que utiliza el reactivo DPD (n-n-dietil-p-fenilendiamina). Es el ensayo más común y es
reconocido oficialmente para la detección del cloro libre. La DPD causa la oxidación del cloro, se produce un cambio de color a magenta (rojo). La
intensidad del color es directamente proporcional a la concentración de cloro.
mg/L: miligramos por litro, son las unidades de concentración, es igual que ppm.
Mol: peso molecular de una sustancia, normalmente expresado en gramos.
Nefelómetro: instrumento utilizado para comparar la turbiedad de soluciones que hace pasar un rayo de luz a través de un tubo transparente y mide
la relación entre la intensidad de la luz dispersa y la luz incidente, en un ángulo de 90º.
Neutralización: adición de un ácido o una base para obtener un pH próximo a 7.
Ozono: oxidante muy energético, con poder oxidante y desinfectante mayor que el cloro. Para la medida y la desinfección con ozono se requiere
inversiones elevadas.
Oxidación: reacción química en la cual el número de oxidación (valencia) de un elemento aumenta debido a la pérdida de uno o más electrones por parte de dicho elemento. La oxidación de un elemento va acompañada por la reducción simultánea del otro elemento.
pH: medición de la concentración de iones hidrógeno o protones (H+) en una solución, expresada como el menos logaritmo decimal de la concentración
de iones hidrógeno expresado en gr/mol/L. La escala de pH va de 0 a 14, los valores menores indican acidez y los mayores alcalinidad. El valor de 7°C
a 25ºC indica la neutralidad.
Potencial REDOX (ORP): Potencial requerido para transferir electrones del oxidante al agente reductor. En el proceso de la oxidación, los electrones
se transfieren de la sustancia que se oxidará al oxidante. Simultáneamente, al oxidarse una sustancia, se reduce otra. Los oxidantes son donantes de
electrones, y los reductores son aceptadores de electrones. Normalmente los oxidantes son cáusticos y los reductores ácidos. La medida del potencial
redox depende del pH.
Reducción: adición de electrones a una sustancia química con el objeto de disminuir su valencia.
Sólidos disueltos totales (TDS): suma de todos los sólidos disueltos volátiles o no volátiles en el agua o en una solución.
Sólidos en suspensión: sólidos insolubles que flotan en la superficie o están en suspensión en el agua, o en otros líquidos.
Turbidez: grado de opacidad producido en el agua por la presencia de partículas en suspensión. Se mide en NTU o FTU.
Tubidímetro: instrumento para medir la turbidez que utiliza como referencia una solución estándar.
Turbiedad: condiciones del agua causada por la presencia de materia en suspensión que produce la dispersión y absorción de luz.
Índice del manual de elaboración de albercas
|












































